○野洲市予防接種実施要綱
平成16年10月1日
告示第179号
(趣旨)
第1条 この告示は、予防接種法(昭和23年法律第68号。以下この条において「法」という。)第5条第1項に規定するA類疾病及びB類疾病に係る定期の予防接種(以下「予防接種」という。)の実施に当たり、法、予防接種法施行令(昭和23年政令第197号。次条第2項及び第3条において「令」という。)、予防接種法施行規則(昭和23年厚生省令第36号。第9条第1号において「施行規則」という。)及び予防接種実施規則(昭和33年厚生省令第27号。第6条第4号において「実施規則」という。)に定めるもののほか、必要な事項を定めるものとする。
(令2告示107・全改、令5告示129・令6告示87・一部改正)
(予防接種の実施)
第2条 市が実施する予防接種の種類、対象者等は次のとおりとする。
種類 | 区分 | 対象者 | 回数 | 接種間隔 |
5種混合(ジフテリア、百日せき、破傷風、急性灰白髄炎、Hib感染症) | 第1期初回 | 生後2月から生後90月に至るまでの間にある者 | 3回 | 20日以上 |
第1期追加 | 第1期初回接種を終了した生後2月から生後90月に至るまでの間にある者 | 1回 | 第1期初回の予防接種終了後6月以上 | |
4種混合(ジフテリア、百日せき、破傷風、急性灰白髄炎) | 第1期初回 | 生後2月から生後90月に至るまでの間にある者 | 3回 | 20日以上 |
第1期追加 | 第1期初回接種を終了した生後2月から生後90月に至るまでの間にある者 | 1回 | 第1期初回の予防接種終了後6月以上 | |
3種混合(ジフテリア、百日せき、破傷風) | 第1期初回 | 生後3月から生後90月に至るまでの間にある者 | 3回 | 20日以上 |
第1期追加 | 第1期初回接種を終了した生後3月から生後90日に至るまでの間にある者 | 1回 | 第1期初回の予防接種終了後6月以上 | |
2種混合(ジフテリア、破傷風) | 第1期初回 | 生後3月から生後90月に至るまでの間にある者 | 2回 | 20日以上 |
第1期追加 | 第1期初回接種を終了した生後3月から生後90月に至るまでの間にある者 | 1回 | 第1期初回の予防接種終了後6月以上 | |
第2期 | 11歳以上13歳未満の者 | 1回 | ||
急性灰白髄炎 | 第1回初回 | 生後3月から生後90月に至る間での間にある者 | 3回 | 20日以上 |
第1期追加 | 第1期初回接種を終了した生後3月から生後90月に至るまでの間にある者 | 1回 | 第1期初回の予防接種終了後6月以上 | |
MR混合(麻しん、風しん) | 第1期 | 生後12月から生後24月に至るまでの間にある者 | 1回 | |
第2期 | 5歳以上7歳未満の者であって、小学校就学の始期に達する日の1年前の日から当該始期に達する日の前日までの間にあるもの | 1回 | ||
麻しん | 第1期 | 生後12月から生後24月に至るまでの間にある者 | 1回 | |
第2期 | 5歳以上7歳未満の者であって、小学校就学の始期に達する日の1年前の日から当該始期に達する日の前日までの間にあるもの | 1回 | ||
風しん | 第1期 | 生後12月から生後24月に至るまでの間にある者 | 1回 | |
第2期 | 5歳以上7歳未満の者であって、小学校就学の始期に達する日の1年前の日から当該始期に達する日の前日までの間にあるもの | 1回 | ||
BCG結核 | 生後12月に至るまでの間にある者 | 1回 | ||
日本脳炎 | 第1期初回 | 生後6月から生後90月に至るまでの間にある者 | 2回 | 6日以上 |
第1期追加 | 第1期初回接種を終了した生後6月から生後90月に至るまでの間にある者 | 1回 | 第1期初回の予防接種後おおむね1年を経過した時期 | |
第2期 | 9歳以上13歳未満の者 | 1回 | ||
Hib感染症 | 初回 | 生後2月から生後90月に至るまでの間にある者で、接種開始時に生後2月から生後7月に至るまでの間にあるもの | 3回 | 27日以上 |
生後2月から生後90月に至るまでの間にある者で、接種開始時に生後7月に至った日の翌日から生後12月に至るまでの間にあるもの | 2回 | 27日以上 | ||
生後2月から生後90月に至るまでの間にある者で、接種開始時に生後12月に至った日の翌日から生後90月に至るまでの間にあるもの | 1回 | |||
追加 | 生後2月から生後90月に至るまでの間にある者で、初回の予防接種の接種開始時に生後2月から生後7月に至るまでの間にあるもの | 1回 | 初回の予防接種後7月以上 | |
生後2月から生後90月に至るまでの間にある者で、初回の予防接種の接種開始時に生後7月に至った日の翌日から生後12月に至るまでの間にあるもの | 1回 | 初回の予防接種の接種後7月以上 | ||
小児の肺炎球菌感染症 | 初回 | 生後2月から生後60月に至るまでの間にある者で、接種開始時に生後2月から生後7月に至るまでの間にあるもの | 3回 | 生後12月に至るまでの間で27日以上 |
生後2月から生後60月に至るまでの間にある者で、接種開始時に生後7月に至った日の翌日から生後12月に至るまでの間にあるもの | 2回 | 生後12月に至る間での間で27日以上 | ||
生後2月から生後60月に至るまでの間にある者で、接種開始時に生後12月に至った日の翌日から生後24月に至るまでの間にあるもの | 2回 | 60日以上 | ||
追加 | 生後2月から生後60月に至るまでの間にある者で、初回の予防接種の開始時に生後2月から生後7月に至るまでの間にあるもの | 1回 | 初回の予防接種の接種後60日以上 | |
生後2月から生後60月に至るまでの間にある者で、初回の予防接種の開始時に生後7月に至った日の翌日から生後12月に至るまでの間にあるもの | 1回 | 生後12月に至った日の翌日以降で初回の予防接種の接種後60日以上 | ||
水痘 | 初回 | 生後12月から生後36月に至るまでの間にある者 | 1回 | |
追加 | 初回接種を終了した生後12月から生後36月に至るまでの間にある者 | 1回 | 初回接種終了後6月から12月に至るまでの間隔をおいて接種 | |
B型肝炎 | 1歳に至るまでの間にある者 | 3回 | 生後2月に至った時から生後9月に至るまでの期間を標準的な接種期間として、27日以上の間隔をおいて2回接種した後、第1回目の接種から139日以上の間隔をおいて1回接種 | |
ロタウイルス感染症 | 経口弱毒生ヒトロタウイルスワクチンを使用する場合は、生後6週に至った日の翌日から、生後24週に至る日の翌日までの間にある者 | 2回 | 27日以上 | |
5価経口弱毒生ロタウイルスワクチンを使用する場合は、生後6週に至った日の翌日から、生後32週に至る日の翌日までの間にある者 | 3回 | 27日以上 | ||
子宮頸がん(ヒトパピローマウイルス感染症)(組換え沈降2価ヒトパピローマウイルス様粒子) | 12歳に至る日の属する年度の初日から16歳となる日の属する年度の末日までの間にある女子 | 3回 | 2回目の接種については1回目の接種後1月以上、3回目については1回目の接種後5月以上 | |
子宮頸がん(ヒトパピローマウイルス感染症)(組換え沈降4価ヒトパピローマウイルス様粒子) | 12歳に至る日の属する年度の初日から16歳となる日の属する年度の末日までの間にある女子 | 3回 | 2回目の接種については1回目の接種後1月以上、3回目については2回目の接種後3月以上 | |
子宮頸がん(ヒトパピローマウイルス感染症)(組換え沈降9価ヒトパピローマウイルス様粒子) | 12歳に至る日の属する年度の初日から16歳となる日の属する年度の末日までの間にある女子 | 3回 | 2回目の接種については1回目の接種後1月以上、3回目については2回目の接種後3月以上 | |
高齢者インフルエンザ | 65歳以上の者 60歳以上65歳未満の者であって、心臓、腎臓又は呼吸器の機能に自己の身辺の日常生活行動が極度に制限される程度の障害を有するもの及びヒト免疫不全ウイルスにより免疫の機能に日常生活がほとんど不可能な程度の障害を有するもの | 毎年度1回(10月1日から12月31日まで) | ||
高齢者肺炎球菌 | ・65歳の者 ・60歳以上65歳未満の者であって、心臓、腎臓又は呼吸器の機能に自己の身辺の日常生活行動が極度に制限される程度の障害を有するもの及びヒト免疫不全ウイルスにより免疫の機能に日常生活がほとんど不可能な程度の障害を有するもの | 1回 | ||
風しん | 第5期 | 昭和37年4月2日から昭和54年4月1日までに生まれた男性 | 1回 | |
新型コロナウイルス感染症 | ・65歳の者 ・60歳以上65歳未満の者であって、心臓、腎臓又は呼吸器の機能に自己の身辺の日常生活行動が極度に制限される程度の障害を有するもの及びヒト免疫不全ウイルスにより免疫の機能に日常生活がほとんど不可能な程度の障害を有するもの | 1回 |
2 前項の表の左欄に掲げる予防接種の種類(高齢者インフルエンザを除く。以下この項において「特定疾病」という。)について、それぞれ同表の右欄に掲げる対象者であった者(当該特定疾病にかかっている者又はかかったことのある者その他令第1条の3第2項の厚生労働省令で定める者を除く。)であって、当該対象者であった間に、同項の厚生労働省令で定める特別の事情があることにより当該特定疾病に係る前項に規定する予防接種を受けることができなかったと認められるものについては、当該特別の事情がなくなった日から起算して2年(高齢者肺炎球菌感染症は1年)を経過する日までの間(令第1条の3第2項の厚生労働省令で定める特定疾病にあっては、同項の厚生労働省令で定める年齢に達するまでの間にある場合に限る。)、当該特定疾病に係る前項に規定する予防接種の対象者とする。
3 第1項に定める予防接種の実施方法及び接種場所は、次のとおりとする。
実施方法 | 接種場所 |
個別接種 | この告示に定める予防接種の実施に関し、野洲市への協力を承諾した守山野洲医師会加入の医療機関 滋賀県予防接種広域化事業への協力を承諾した滋賀県医師会加入の医療機関及び滋賀県病院協会加入の医療機関 この告示に定める予防接種の実施に関し、野洲市と当該予防接種に係る委託契約を締結した介護老人福祉施設等 |
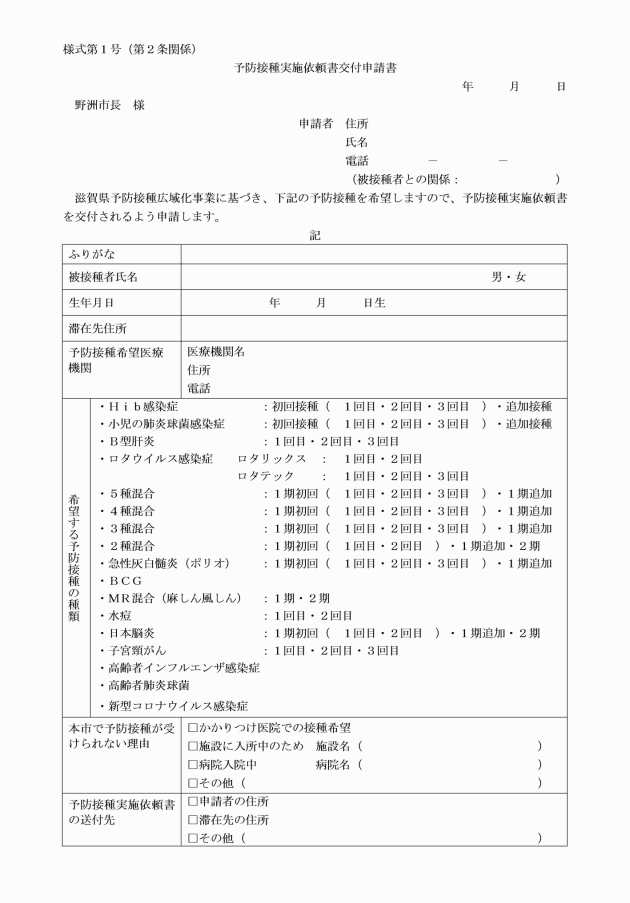
4 滋賀県予防接種広域化事業に基づく予防接種を希望する者は、事前に予防接種実施依頼書交付申請書(様式第1号)を市長に提出しなければならない。
6 第3項の規定にかかわらず、市長は、特に必要があると認めるときは、実施方法及び接種場所を別に定めて、予防接種を行うことができる。
(平26告示104・全改、平27告示135・平28告示166・平31告示21・令2告示107・令5告示129・令6告示87・一部改正)
(対象者に対する周知等)
第3条 市長は、予防接種を行おうとするときは、令第5条の規定に基づき、次の事項を公告するものとする。
(1) 予防接種の種類
(2) 予防接種の対象者
(3) 予防接種を行う期日又は期間及び場所
(4) 予防接種を受けるに当たって注意すべき事項
(5) 前各号に掲げるもののほか、必要な事項
2 市長は、令第6条の規定に基づき、予防接種の対象者又はその保護者に対し、前項各号に掲げる事項を、市の広報、ホームページその他適切な方法により周知するものとする。
(平27告示135・追加)
(接種液)
第4条 接種液の取扱い等については、次に掲げるとおりとする。
(1) 接種液の使用前には、国家検定に合格したことを示す検定証紙の有無、表示された接種液の種類、有効期限を確認し、異常な混濁、着色異物の混入その他の異常が無いかを点検する。
(2) 接種液の貯蔵は、それぞれの生物学的製剤基準の定めるところによるものとし、その方法は、遮光して所定の温度が保たれていることを温度計により確認できる冷蔵庫等を使用する。経口生ポリオワクチンは原則としてフリーザーに保存し、マイナス20度以下の貯蔵条件を維持する。
(平27告示135・旧第3条繰下)
(平26告示104・一部改正、平27告示135・旧第4条繰下・一部改正)
(予診、接種不適当者及び接種要注意者)
第6条 予診、接種不適当者及び接種要注意者の確認は、次により行うものとする。
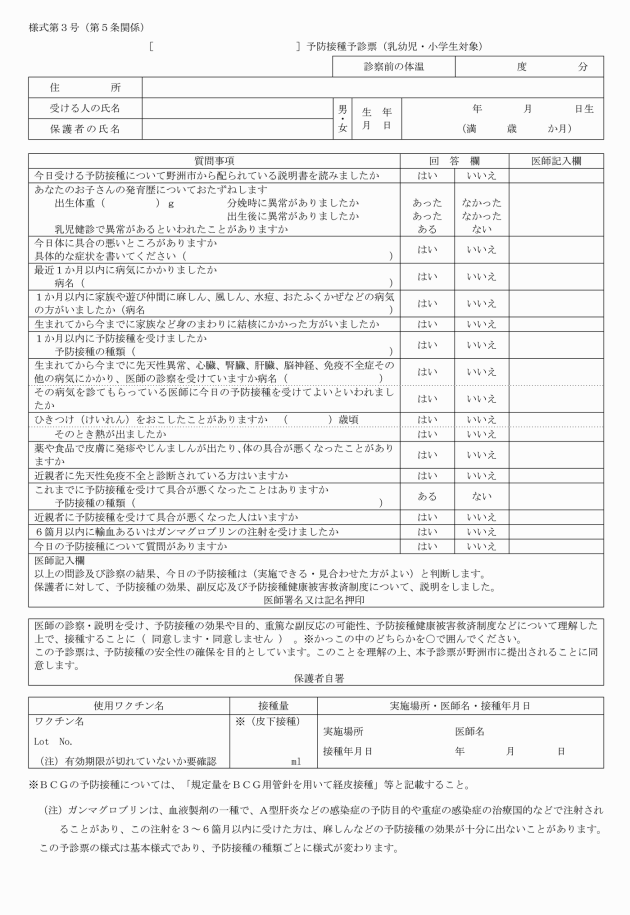
(1) 問診については、あらかじめ予防接種予診票を配布し、各項目について記載の上、これを接種の際に持参するよう指導する。なお、予診票は予防接種の種類により異なる紙色のものを使用する。
(2) 乳幼児に対して予防接種を行う場合には、その保護者に対し、接種前に母子健康手帳の提示を求める。
(3) 接種施設において、問診・検温・視診・聴診等の診察を接種前に行い、接種を受けることが不適当な者又は接種の判断を行うに際し注意を要する者に該当するかどうかを確認する。
(4) 予診票の結果異常が認められ、かつ、実施規則第6条に規定する、接種を受けることが不適当な者に対しては、当日は接種を行わず、必要がある場合は精密検査を受けるよう指示する。
(5) 接種の判断を行うに際し注意を要する者については、被接種者の健康状態及び体質を勘案し、注意して接種することが必要である。なお、接種の判断を行うに際し、注意を要するものは次のとおりとする。
ア 心臓血管系疾患、腎臓疾患、肝臓疾患、血液疾患及び発育障害等の基礎疾患を有することが明らかな者
イ 前回の予防接種で2日以内に発熱の見られた者又は全身性発疹等のアレルギーを疑う症状を呈したことがある者
ウ 過去にけいれんの既往のある者
エ 過去に免疫不全の診断がなされている者
オ 接種しようとする接種液の成分に対して、アレルギーを呈するおそれのある者
(6) 予診の際は、予防接種後に起こり得る副反応、コッホ現象及び予防接種健康被害救済制度について十分に説明し、保護者がその内容を理解した上で、予防接種実施に関する明示の同意をした場合に限り接種を行うものとする。
(平17告示39・平26告示104・一部改正、平27告示135・旧第5条繰下)
(接種時の注意)
第7条 接種時は、次のことに注意する。
(1) 予防接種を行うに当たっては、次の事項を遵守すること。
ア 予防接種に従事する者は、手指を消毒すること。
イ ワクチンによって、凍結させないこと、溶解は接種直前に行い一度溶解したものは直ちに使用すること、溶解の前後にかかわらず光が当たらないよう注意することなどの留意事項があるので、それぞれ添付文書を確認の上、適切に使用すること。
ウ 接種液の使用に当たっては、有効期限内のものを均質にして使用すること。
エ バイアル入りの接種液は、栓及びその周囲をアルコール消毒した後、栓を取り外さないで吸引すること。
オ 接種液が入っているアンプルを開口するときは、開口する部分をあらかじめアルコール消毒すること。
カ 沈降精製百日せきジフテリア破傷風不活化ポリオヘモフィルスb型混合ワクチン(以下「5種混合ワクチン」という。)を使用するジフテリア、百日せき、急性灰白髄炎、破傷風及びHib感染症、沈降15価肺炎球菌結合型ワクチンを使用する肺炎球菌感染症並びに結核、ヒトパピローマウイルス感染症、ロタウイルス感染症、高齢者の肺炎球菌感染症及び新型コロナウイルス感染症以外の予防接種にあっては、原則として上腕伸側に皮下接種により行うこと。この場合において、接種前には接種部位をアルコール消毒し、同一部位への反復しての接種は避けること。
キ 5種混合ワクチンを使用するジフテリア、百日せき、急性灰白髄炎、破傷風及びHib感染症及び沈降15価肺炎球菌結合型ワクチンを使用する肺炎球菌感染症の予防接種にあっては、皮下接種又は筋肉内注射により行うこと。また、接種部位については、皮下接種の場合は上腕伸側(外側)、筋肉注射の場合は三角筋部又は大腿四頭筋部(ただし、乳児にあっては三角筋部ではなく大腿四頭筋部)にそれぞれ行うこと。この場合において、接種前には接種部位をアルコール消毒し、接種に際しては、注射針の先端が血管内に入っていないことを確認し、同一部位への反復しての接種は避けること。
ク 結核の予防接種にあっては、接種前に接種部位をアルコール消毒し、接種に際しては接種部位の皮膚を緊張させ、ワクチンの懸濁液を上腕外側のほぼ中央部に滴下塗布し、9本針植付けの経皮用接種針(管針)を接種皮膚面に対してほぼ垂直に保ちこれを強く圧して行うこと。この場合において、接種数は2箇とし、管針の円跡は相互に接するものとすること。
ケ ヒトパピローマウイルス感染症の予防接種にあっては、ワクチンの添付文書の記載に従って、組換え沈降2価ヒトパピローマウイルス様粒子ワクチンを使用する場合は原則として上腕の三角筋部に、組換え沈降4価ヒトパピローマウイルス様粒子ワクチンを使用する場合は原則として上腕の三角筋部又は大腿四頭筋部に筋肉内注射し、組換え9価ヒトパピローマウイルス様粒子ワクチンを使用する場合は原則として上腕の三角筋部に筋肉注射することとし、当該部位への接種が困難な場合は、大腿前外側部への接種を考慮すること。この場合において、臀部には接種しないこととし、接種前に接種部位をアルコール消毒し、接種に際しては注射針の先端が血管内に入っていないことを確認し、同一部位への反復しての接種は避けること。
コ ロタウイルス感染症の予防接種にあっては、母子健康手帳等により接種記録を確認の上、原則として同一ワクチンを複数回(経口弱毒生ヒトロタウイルスワクチンは2回、五価経口弱毒生ロタウイルスワクチンは3回)接種し、接種に際しては接種液が封入されている容器より直接、全量をゆっくりと経口投与すること。この場合において、他の薬剤や溶液と混合してはならない。
サ 高齢者の肺炎球菌感染症の予防接種にあっては、原則として上腕伸側に皮下接種又は上腕の三角筋部に筋肉内注射により行うこと。この場合において、接種前には接種部位をアルコール消毒し、接種に際しては注射針の先端が血管内に入っていないことを確認すること。
シ 新型コロナウイルス感染症の予防接種にあっては、原則として上腕の三角筋部に筋肉内注射により行うこと。この場合において、接種前には接種部位をアルコール消毒し、接種に際しては注射針の先端が血管内に入っていないことを確認すること。
ス 接種用具等の消毒は、適切に行うこと。
(2) 予防接種を受けた者又はその保護者に対して、次の事項を知らせる。
ア 接種時には、接種部位を清潔に保ち、接種当日は過激な運動を避けるよう注意すること。
イ 接種後、局所の異常反応や体調の変化を訴える場合には、速やかに医師の診察を受けること。
ウ 被接種者又はその保護者は、イの場合において、被接種者が医師の診察を受けたときは、速やかに市長に連絡すること。
(平27告示135・旧第6条繰下、令2告示107・令5告示129・令6告示87・一部改正)
(予防接種済証等の交付)
第8条 医療機関の医師は、乳幼児から高等学校相当の年齢の者までのものに予防接種を行ったときは、被接種者又はその保護者に対し、予防接種済証を交付し、又は母子健康手帳に予防接種及びワクチンの種類、接種年月日その他の証明すべき事項を記載することをもってその交付に代えることができる。
(令6告示87・全改)
(健康被害発生時の報告)
第9条 健康被害発生時の報告は、次に掲げるとおりとする。
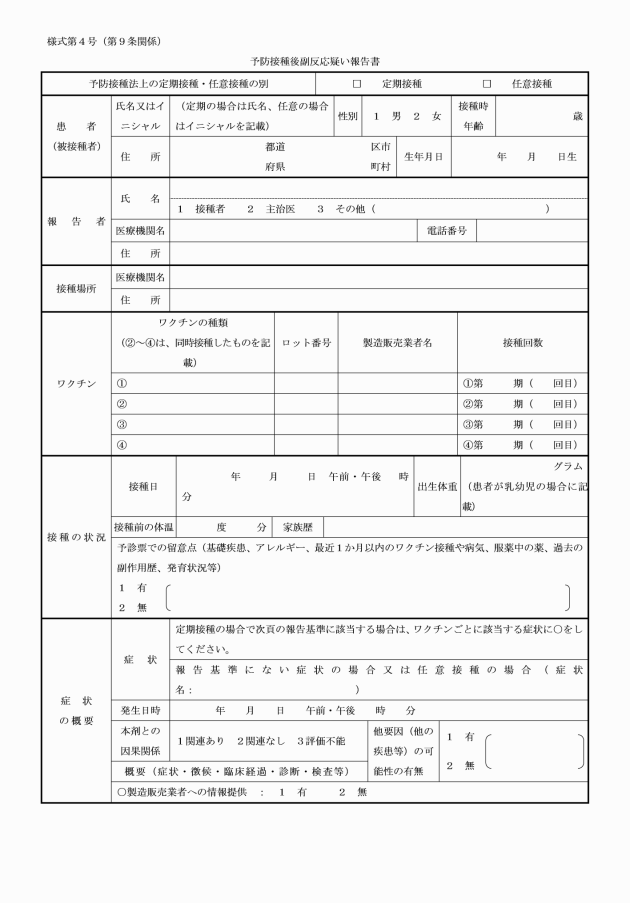
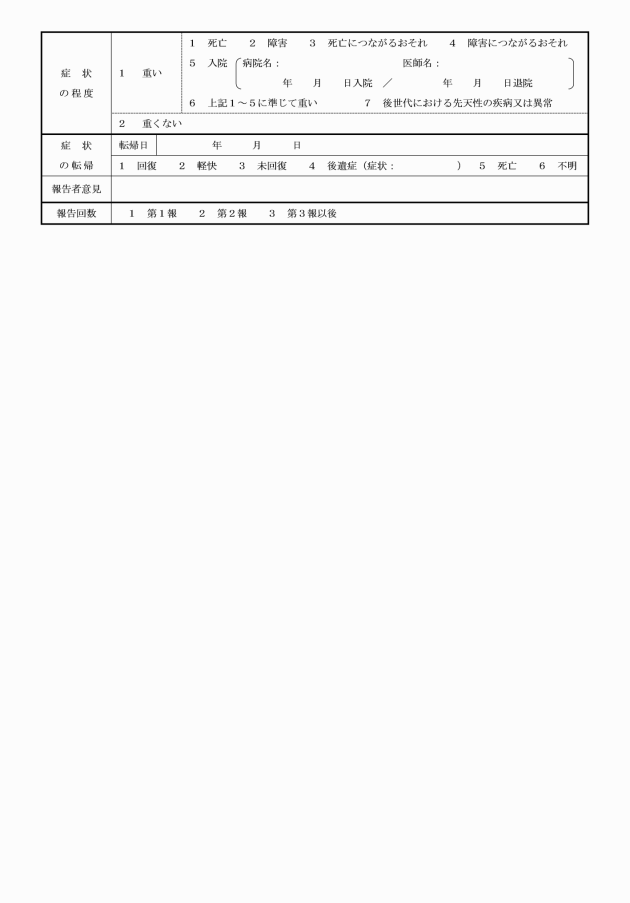
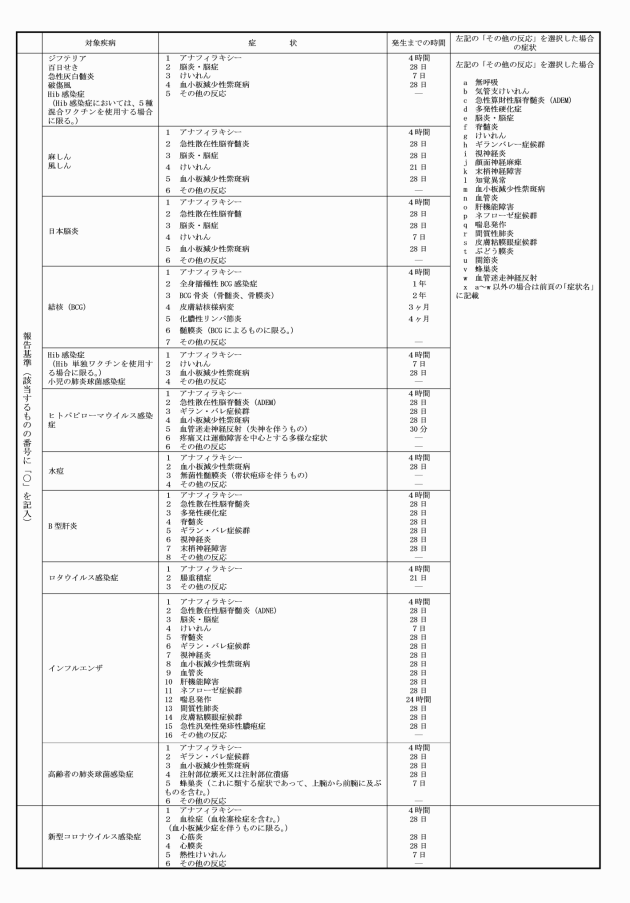
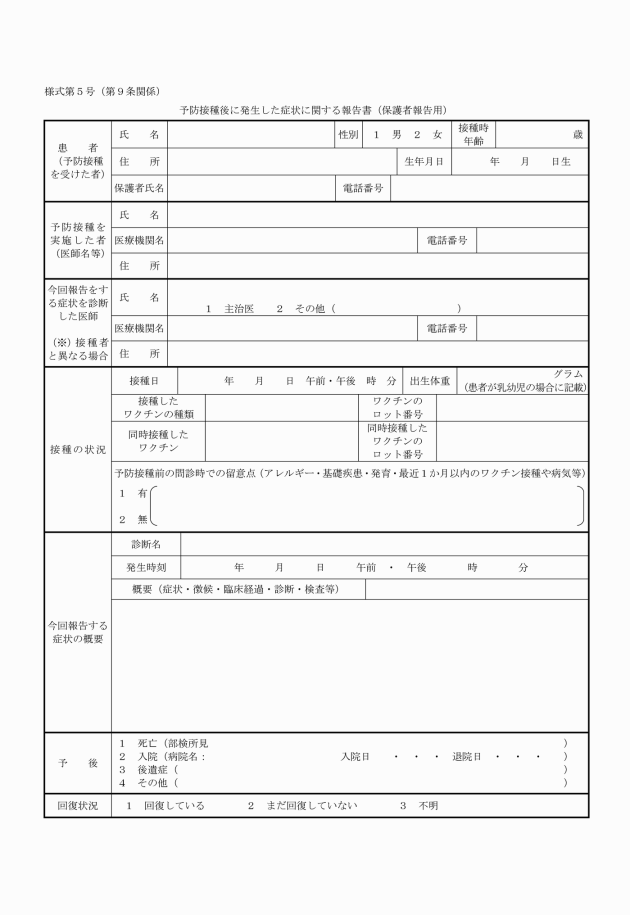
(2) 市長は、被接種者又はその保護者から定期の予防接種後に発生した健康被害に関し相談を受けた場合は、必要に応じて、被接種者又はその保護者に対して、予防接種後に発生した症状に関する報告書(様式第5号)を提出するように促すとともに、それを、滋賀県知事を通じて厚生労働省健康局結核感染症課へ報告するものとする。この場合において、市長は当該健康被害を診断した医師に対して、副反応疑い報告書の提出を促すとともに、医師が報告基準に該当せず、因果関係もないと判断し、副反応疑い報告書を提出しない場合は、その理由も添えて厚生労働省健康局結核感染症課に報告するものとする。
(平26告示104・全改、平27告示135・旧第8条繰下・一部改正、令5告示129・令6告示87・一部改正)
(他の予防接種との関係)
第10条 他の予防接種との関係は、次に掲げるとおりとする。
(1) 乾燥弱毒性麻しん風しん混合ワクチン、乾燥弱毒性麻しんワクチン、乾燥弱毒性風しんワクチン、経皮接種用乾燥BCGワクチン又は乾燥弱毒性水痘ワクチンを接種した日から、乾燥弱毒性麻しん風しん混合ワクチン、乾燥弱毒性麻しんワクチン、乾燥弱毒性風しんワクチン、経皮接種用BCGワクチン又は乾燥弱毒性水痘ワクチンの予防接種(同一種類のワクチンを接種する場合において、接種の間隔に関する定めがある場合は、その定めるところによる。)を行うまでの間隔は、27日以上おくこと。
(2) 2種類以上の予防接種を同時に同一の接種対象者に対して行う同時接種(混合ワクチン・混合トキソイドを使用する場合は、1つのワクチンと数え、同時接種としては扱わない。)は、医師が特別に必要と認めた場合に行うことができること。
(平17告示39・一部改正、平27告示135・旧第9条繰下、令2告示107・一部改正)
(コッホ現象に係る報告)
第11条 結核既感染後にBCGを接種した場合に見られるコッホ現象が被接種者に見られた場合の報告は、次に掲げるとおりとする。
(1) 市長は、あらかじめ予防接種後コッホ現象事例報告書(様式第6号)を医療機関に配布し、医師がコッホ現象を診断した場合は、保護者の同意を得て、直ちに市長へ報告するよう医療機関に協力を求めるものとする。
(平17告示39・追加、平26告示104・一部改正、平27告示135・旧第10条繰下・一部改正、令5告示129・一部改正)
(予防接種時の事故の報告)
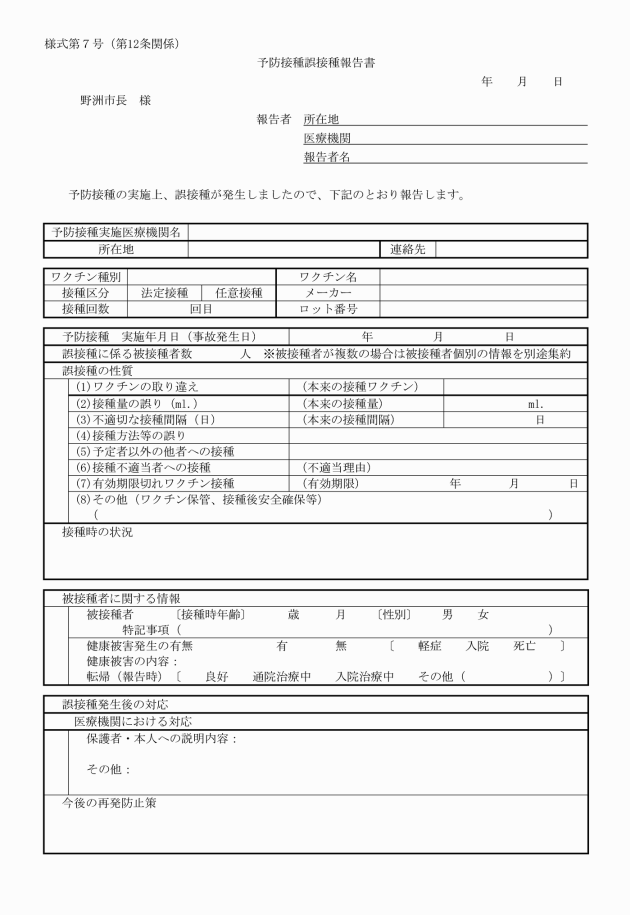
第12条 市長は、あらかじめ予防接種誤接種報告書(様式第7号)を医療機関に配布し、予防接種の誤接種の発生があった場合は、速やかに市長へ報告するよう医療機関に協力を求めるものとする。
(1) 予防接種を実施した機関
(2) ワクチンの種類、メーカー、ロット番号
(3) 予防接種を実施した年月日(事故発生日)
(4) 事故に係る被接種者数
(5) 事故の概要と原因
(6) 市長の講じた事故への対応
(7) 健康被害発生の有無
(8) 今後の再発防止策
(9) 市担当者の連絡先(電話番号、メールアドレス等)
(平27告示135・追加、令2告示107・令5告示129・一部改正)
(その他)
第13条 この告示に定めるもののほか、予防接種に必要な事項は、市長が別に定める。
(平26告示104・全改、平27告示135・旧第11条繰下)
付則
(施行期日)
1 この告示は、平成16年10月1日から施行する。
(経過措置)
2 この告示の施行の日の前日までに、合併前の野洲町予防接種実施要綱(平成8年野洲町告示第27号)の規定によりなされた決定、手続その他の行為は、この告示の相当規定によりなされたものとみなす。
(子宮頸がんの予防接種に係る経過措置)
3 令和4年4月1日から令和7年3月31日までの間は、第2条の表中子宮頸がん(ヒトパピローマウイルス感染症)(組換え沈降2価ヒトパピローマウイルス様粒子)の部中「12歳に至る日の属する年度の初日から16歳となる日の属する年度の末日までの間にある女子」とあるのは「12歳に至る日の属する年度の初日から16歳となる日の属する年度の末日までの間にある女子。ただし、令和4年4月1日から令和7年3月31日までの間は、平成9年4月2日から平成20年4月1日までの間に生まれた女子でヒトパピローマウイルス感染症(組換え沈降2価ヒトパピローマウイルス様粒子)の予防接種が終了していない者も対象とする。」と、同表子宮頸がん(ヒトパピローマウイルス感染症)(組換え沈降4価ヒトパピローマウイルス様粒子)の部中「12歳に至る日の属する年度の初日から16歳となる日の属する年度の末日までの間にある女子」とあるのは「12歳に至る日の属する年度の初日から16歳となる日の属する年度の末日までの間にある女子。ただし、令和4年4月1日から令和7年3月31日までの間は、平成9年4月2日から平成20年4月1日までの間に生まれた女子でヒトパピローマウイルス感染症(組換え沈降4価ヒトパピローマウイルス様粒子)の予防接種が終了していない者も対象とする。」と、同表子宮頸がん(ヒトパピローマウイルス感染症)(組換え沈降9価ヒトパピローマウイルス様粒子)の部中「12歳に至る日の属する年度の初日から16歳となる日の属する年度の末日までの間にある女子」とあるのは「12歳に至る日の属する年度の初日から16歳となる日の属する年度の末日までの間にある女子。ただし、令和5年4月1日から令和7年3月31日までの間は、平成9年4月2日から平成20年4月1日までの間に生まれた女子でヒトパピローマウイルス感染症(組換え沈降9価ヒトパピローマウイルス様粒子)の予防接種が終了していない者も対象とする。」と読み替えるものとする。
(令4告示72・追加、令5告示129・一部改正)
付則(平成17年告示第39号)
この告示は、平成17年4月1日から施行する。
付則(平成18年告示第140号)
この告示は、平成18年9月15日から施行し、改正後の野洲市予防接種実施要綱は、平成18年6月2日から適用する。
付則(平成26年告示第104号)
(施行期日)
1 この告示は、平成26年10月1日から施行する。
(野洲市高齢者インフルエンザ予防接種実施要綱等の廃止)
2 次に掲げる要綱は、廃止する。
(1) 野洲市高齢者インフルエンザ予防接種実施要綱(平成16年野洲市告示第178号)
(2) 野洲市子宮頸がん等ワクチン接種事業実施要綱(平成23年野洲市告示第11号)
付則(平成27年告示第135号)
この告示は、平成27年7月24日から施行し、改正後の野洲市予防接種実施要綱の規定は、同年4月1日から適用する。
付則(平成28年告示第166号)
(施行期日)
1 この告示は、平成28年10月1日から施行する。
(平成28年10月1日前の予防接種に係る経過措置)
2 この告示の施行前の予防接種であって、改正後の野洲市予防接種実施要綱の規定による定期のB型肝炎の予防接種に相当するものについては当該予防接種を定期のB型肝炎の予防接種とみなし、当該予防接種を受けた者については定期のB型肝炎の予防接種を受けた者とみなして、以降の予防接種を行うものとする。
付則(平成31年告示第21号)
この告示は、平成31年4月1日から施行する。
付則(令和2年告示第107号)
(施行期日)
1 この告示は、令和2年10月1日から施行する。
(経過措置)
2 この告示による改正後の第2条第1項の規定(同項の表ロタウイルス感染症の項に係る部分に限る。)は、令和2年8月1日以後に生まれた者について適用する。
付則(令和4年告示第72号)
この告示は、令和4年4月1日から施行する。
付則(令和5年告示第129号)
この告示は、令和5年4月1日から施行する。
付則(令和6年告示第87号)
(施行期日)
1 この告示は、令和6年4月1日から施行する。
(経過措置)
2 この告示の施行の際、改正前の野洲市予防接種実施要綱様式第1号、様式第2号及び様式第4号に規定する様式で、現に残存するものは、当分の間、所要の修正を加え、なお使用することができるものとする。
(平27告示135・追加、平28告示166・令2告示107・令6告示87・一部改正)
(平27告示135・追加、平28告示166・令2告示107・令6告示87・一部改正)
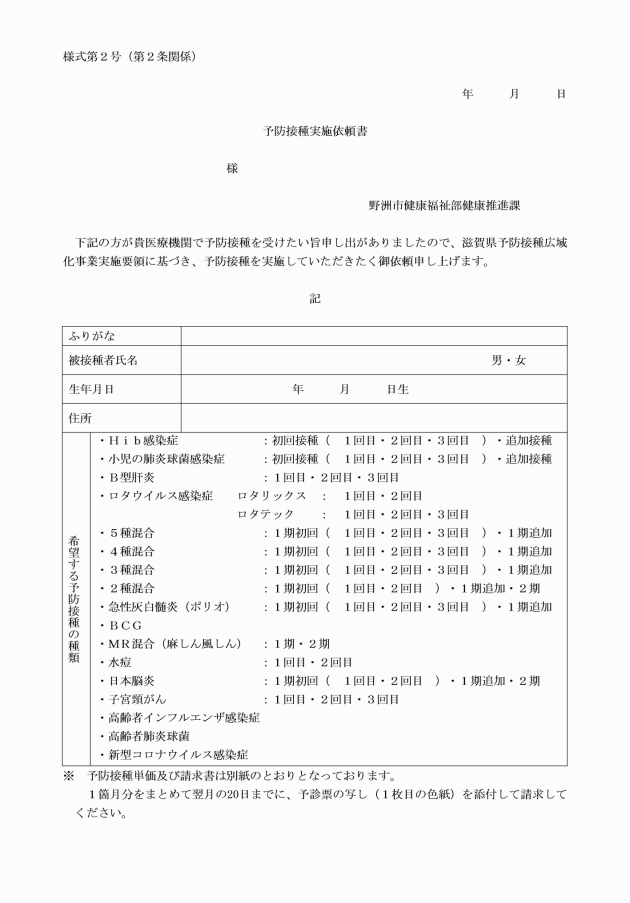
(平26告示104・全改、平27告示135・旧様式第1号繰下・一部改正、平31告示21・一部改正)
(令6告示87・全改)

(平26告示104・全改、平27告示135・旧様式第3号繰下・一部改正、平31告示21・一部改正)
(平26告示104・追加、平27告示135・旧様式第4号繰下・一部改正、平31告示21・一部改正)

(平27告示135・追加)
(平27告示135・追加、平31告示21・令2告示107・一部改正)
